Las Mezclas
- Obtener vínculo
- X
- Correo electrónico
- Otras apps
La mezcla
Una mezcla es un material compuesto por dos o más componentes unidos físicamente, pero no químicamente. Esto significa que no se produce entre ellos ninguna reacción química, es decir, que cada componente mantiene su identidad y sus propiedades químicas, incluso en el caso en que no podamos distinguir un componente del otro.
Los componentes o fases de una mezcla se hallan unidos mecánica o físicamente. Por eso, a menudo se ven alteradas sus propiedades físicas, como el punto de ebullición o de fusión.
Sin embargo, al no producirse cambios químicos permanentes, es posible emplear mecanismos físicos de separación para extraer cada uno de los componentes de una mezcla. Dichos mecanismos físicos suelen ser térmicos (cuando involucran calor) o mecánicos (cuando involucran el desplazamiento o el movimiento).
Las mezclas son formas mixtas de la materia sumamente frecuentes en la vida cotidiana, y muchos de los materiales que usamos son el resultado de un procedimiento de mezclado o mixtura. Los componentes de una mezcla pueden hallarse en distintos estados de agregación (sólidos, líquidos, gaseosos, plasmas, o combinaciones entre ellos).
Características
Tienen composiciones variables
Sus componentes pueden ser separados:
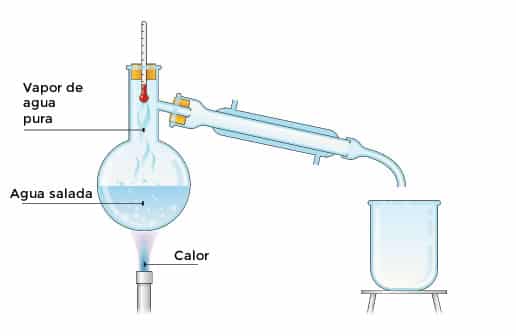
- Destilación: la separación de mezclas se obtiene por las diferencias propias de los puntos de ebullición.
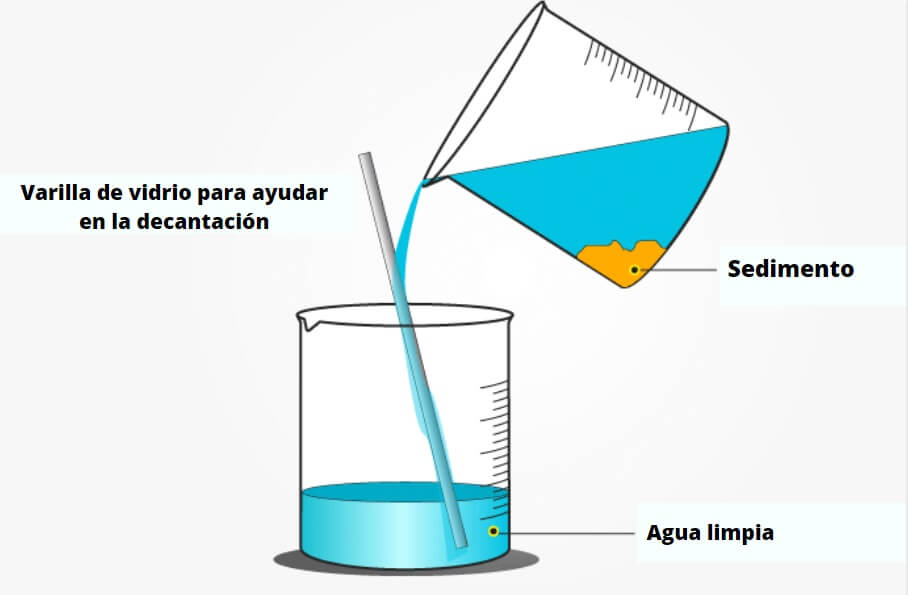
- Decantación: se utiliza para separar a los líquidos inmiscibles y a los sólidos en suspensión.
- Filtración: se usa para la separación de partículas sólidas muy pequeñas que se hayan suspendidas en materiales líquidos.
- Tienen reactividad: Algunas mezclas pueden resultar reactivas bajo ciertas condiciones. Por ejemplo, en un motor de combustión interna, la nafta o el gasoil se mezclan con el aire y eso inicia la ignición del motor.
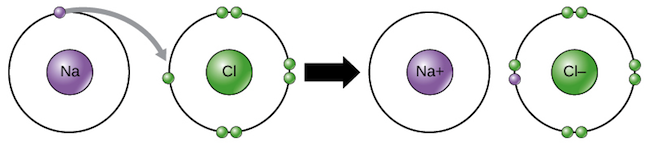
- No producen la formación de enlaces químicos: Debe quedar en claro que una mezcla no es una sustancia química, lo que quiere decir que no se origina a consecuencia de reacciones químicas. Es por ello que no hay cambio energético neto en el proceso de mezcla, aunque en algunas disoluciones se produce liberación de calor, que puede llegar a ser muy intensa (como cuando se trata de hacer una solución de ácido sulfúrico o de hidróxido de sodio).
- Presentan cambios en algunas propiedades físicas: Las sustancias que integran la mezcla conservan su naturaleza química, pero algunas propiedades físico-químicas de la fase dispersante pueden variar a causa de la presencia de la fase dispersa. Por ejemplo, el punto de ebullición del agua aumenta y su punto de congelación disminuye al agregar un soluto. Este fenómeno se conoce como “descenso crioscópico” y es importante tenerlo en cuenta en la fabricación de diversos productos.
- No poseen fórmula química: No se pueden representar mediante una fórmula química. Al no estar compuestas por proporciones definidas de los elementos que la integran, las mezclas no se pueden expresar mediante una fórmula, como sí sucede con las sustancias de composición conocida.
Las mezclas resultan gracias a combinar sustancias en algunas condiciones como presión, calor, etcétera. Por esta razón, también se recuperan y se separan usando procedimientos mecánicos o físicos tales como la centrifugación o la filtración. Los métodos más utilizados en la separación de mezclas son los explicados a continuación:
Existen mezclas que bajo algunas condiciones son reactivas. Un ejemplo de la reactividad de las mezclas es cuando el gasoil o la nafta de un motor de combustión interna son mezcladas con el aire, dando inicio a la ignición del motor.
Se debe tener siempre presente que una mezcla no es igual a una sustancia química, esto significa que la mezcla no es originada a causa de reacciones químicas. Queriendo decir que no existe un cambio neto energético en el procedimiento de la mezcla, aunque se da una liberación de calor en algunas disoluciones la cual puede ser bastante intensa; como cuando se intenta realizar una solución de hidróxido de sodio o de ácido sulfúrico.
Las sustancias que forman parte de la mezcla mantienen su naturaleza química pero pueden variar en algunas propiedades químicas y físicas por la fase dispersa presente. Un ejemplo es cuando disminuye el punto de congelación y aumenta el punto de ebullición en el agua al añadir un soluto. Este fenómeno es conocido como descenso crioscópico y es de vital importancia tenerlo presente al fabricar algunos productos.
Las mezclas no se representan con fórmulas químicas. Las mezclas no pueden expresarse a través de una fórmula porque no se componen de proporciones definidas sobre los elementos que las integran, como sí ocurre con las sustancias cuya composición es conocida.
Tipos de mezclas
- Obtener vínculo
- X
- Correo electrónico
- Otras apps








Comentarios
Publicar un comentario